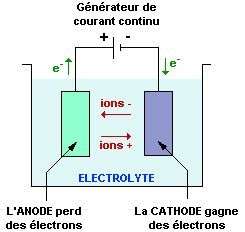
L’électrolyse est un processus chimique qui permet la décomposition de certaines substances lorsque celles-ci sont soumises à un courant électrique. Il s’agit d’une réaction qui se déroule dans une cuve contenant un électrolyte, une substance conductrice capable de se dissocier en ions. Dans cette cuve, deux électrodes sont plongées et elles sont reliées aux bornes d’un générateur de courant continu.
Anode et cathode : les rôles des électrodes
Une fois que le courant électrique est enclenché, la première électrode, appelée anode, est reliée à la borne positive du générateur. Cette électrode est celle où se produisent les réactions d’oxydation, c’est-à-dire la perte d’électrons. Les ions présents dans l’électrolyte se dirigent alors vers l’anode et y subissent des transformations chimiques.
De l’autre côté de la cuve se trouve la seconde électrode, appelée cathode, reliée à la borne négative du générateur. Cette électrode est le lieu des réactions de réduction, c’est-à-dire le gain d’électrons. Les ions provenant de l’électrolyte se déplacent vers la cathode et subissent également des transformations chimiques.
Applications de l’électrolyse
L’électrolyse trouve de nombreuses applications dans de nombreux domaines, notamment l’industrie et la chimie.
En métallurgie, par exemple, l’électrolyse est utilisée pour purifier ou extraire certains métaux. L’électrolyse de l’aluminium est un procédé industriel couramment utilisé dans la production de ce métal. Grâce à ce processus, il est possible d’obtenir de l’aluminium pur à partir d’un minerai appelé bauxite.
En chimie, l’électrolyse est utilisée pour réaliser des analyses qualitatives et quantitatives des substances. Elle permet également la synthèse de nouveaux composés chimiques. Par exemple, l’électrolyse de l’eau permet d’obtenir de l’hydrogène et de l’oxygène, qui peuvent ensuite être utilisés dans diverses applications industrielles ou énergétiques.
Les avantages et les inconvénients de l’électrolyse
L’électrolyse présente de nombreux avantages, notamment sa capacité à produire des substances pures et à haute densité énergétique. Elle permet également de contrôler efficacement les réactions chimiques en ajustant les paramètres tels que la tension, le courant et le temps de réaction.
Cependant, l’électrolyse présente également certains inconvénients. Tout d’abord, elle nécessite une source d’énergie électrique, ce qui peut être coûteux et polluant si celle-ci est générée à partir de sources non renouvelables. De plus, certaines substances peuvent être toxiques ou corrosives, ce qui nécessite des précautions particulières lors de la manipulation.
Conclusion
L’électrolyse est un processus chimique essentiel qui permet la décomposition de substances grâce à l’application d’un courant électrique. Ce processus trouve de nombreuses applications pratiques dans divers domaines, offrant la possibilité de produire des substances pures et d’effectuer des réactions chimiques contrôlées. Cependant, il est important de prendre en compte les avantages et les inconvénients de l’électrolyse afin de l’utiliser de manière responsable et efficace.